医学多模态人工智能的技术挑战与临床应用综述:基于432篇文献 2018-2024 的研究分析
数据模态使用情况概览
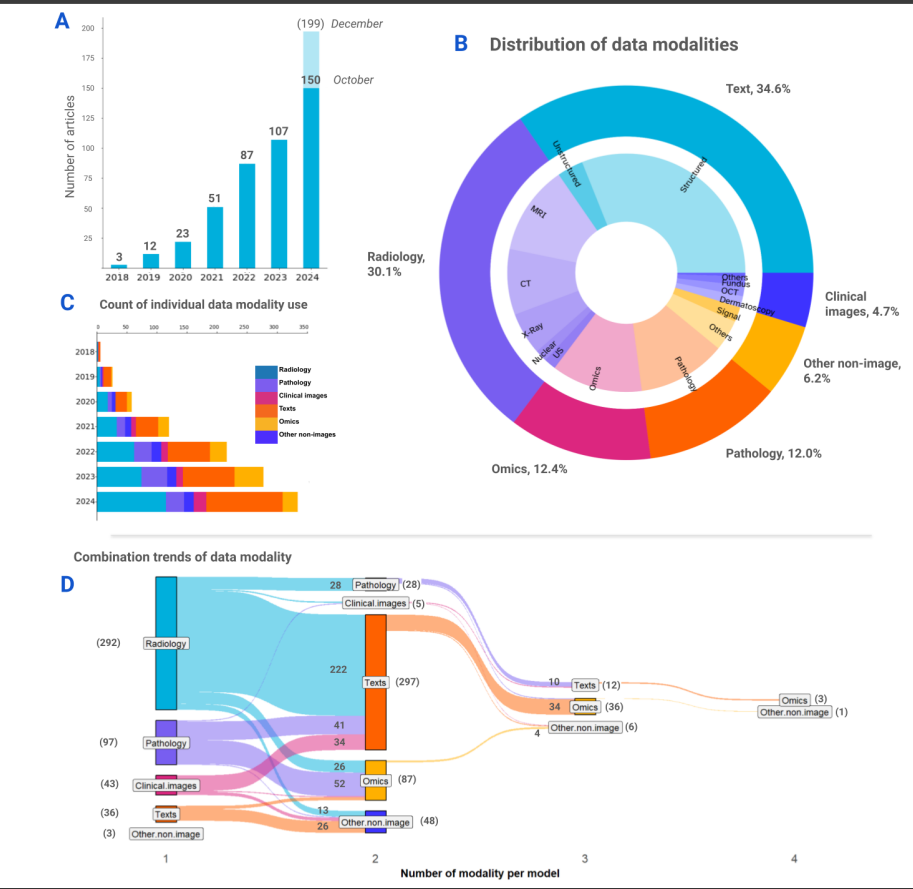
(A) 按年份分布的文章数量条形图
- 显示2018-2024年间文章数量的指数增长
- 从2018年的3篇增长到2024年的150篇
(B) 数据模态分布饼图
- 显示不同模态的占比:文本(34.6%)、放射学(30.1%)、病理学(12.0%)、组学(12.4%)等
- 详细展示各模态的子类型
© 各年份数据模态使用统计堆叠图
- 展示不同模态随时间的使用趋势
- 放射学和文本数据持续占主导地位
(D) 模态组合趋势图
- 展示不同模态之间的组合情况
- 放射学与文本的组合最为常见(n=206)
- 展示了双模态、三模态和四模态的组合情况
医学任务和数据来源深入分析
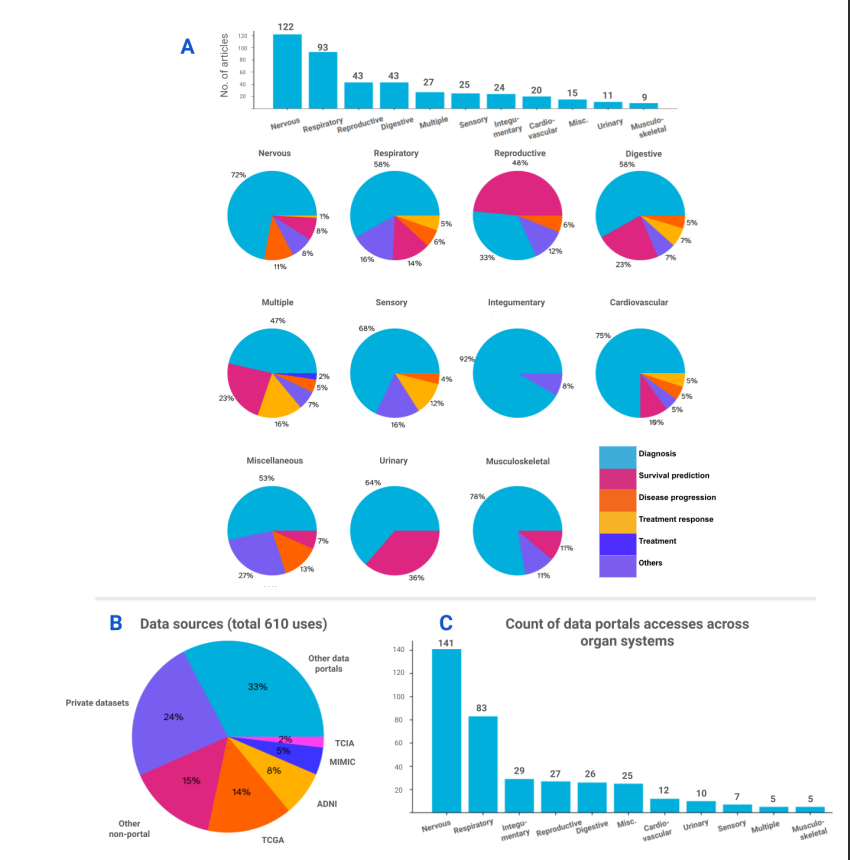
(A) 器官系统和医学任务分布
- 上部:展示各器官系统的研究数量
- 下部:各系统中不同医学任务的占比饼图
- 神经系统(122篇)和呼吸系统(93篇)研究最多
(B) 数据来源分布饼图
- 显示公共数据集、私有数据集等不同来源的占比
- 61%来自公共数据门户
© 各器官系统的公共数据使用情况条形图
- 展示不同器官系统研究中公共数据的使用频率
- 神经系统(141次)和呼吸系统(83次)使用最多
不同融合阶段示意图
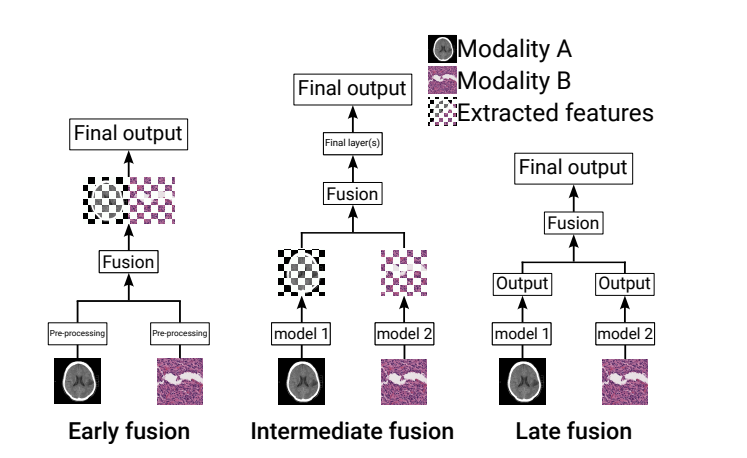
- 展示了早期融合、中期融合和晚期融合三种模态融合策略
- 通过流程图说明了不同融合方式的数据处理流程
- 清晰展示了各个融合阶段的特点和差异
论文大纲
├── 1 多模态AI发展概述【研究背景】
│ ├── 医疗数据的爆发性增长【发展驱动】
│ │ ├── 数字病理学【数据来源】
│ │ ├── 生物传感器【数据来源】
│ │ └── 下一代测序【数据来源】
│ └── 多模态AI的优势【技术价值】
│ ├── 数据互补性【核心特征】
│ └── 决策全面性【核心特征】
├── 2 技术架构【核心内容】
│ ├── 特征编码方法【技术实现】
│ │ ├── CNN【编码方式】
│ │ ├── ViT【编码方式】
│ │ └── RNN【编码方式】
│ └── 模态融合策略【技术实现】
│ ├── 早期融合【融合方式】
│ ├── 中期融合【融合方式】
│ └── 晚期融合【融合方式】
├── 3 应用领域【实践应用】
│ ├── 神经系统【应用场景】
│ ├── 呼吸系统【应用场景】
│ ├── 消化系统【应用场景】
│ └── 生殖系统【应用场景】
└── 4 临床实施挑战【未来发展】
├── 数据孤岛问题【技术挑战】
├── 隐私安全问题【伦理挑战】
└── 模型解释性问题【可信度挑战】
理解
- 背景和问题:
背景类别:医疗数据整合与决策支持
具体问题:
- 医疗数据来源日益多样化(影像、病理、基因等),但数据分散在不同部门
- 临床决策需要综合多个维度信息,单一模态AI模型无法满足需求
- 多模态数据整合面临技术挑战(数据特征不一致、缺失值处理等)
- 概念性质:
多模态AI是一种融合多源医疗数据的智能系统
性质由以下因素决定:
- 数据互补性:不同模态数据提供不同维度的病情信息
- 特征异质性:不同模态数据具有不同的数据结构和特征
- 整合复杂性:需要处理数据缺失、对齐等技术难题
-
对比案例:
正例:将CT影像、病理切片和临床指标结合,提高肺癌诊断准确率
反例:仅使用CT影像预测肺结节良恶性,忽略其他临床信息 -
类比理解:
多模态AI就像一个经验丰富的医生团队:
- 影像科医生(影像数据分析)
- 病理科医生(病理切片分析)
- 临床医生(症状体征分析)
每个专家提供各自专业视角,最后通过多学科会诊形成综合诊断意见。
-
概念介绍与总结:
多模态AI是一种将多源异构医疗数据进行智能整合的技术系统,通过特征提取、模态融合等方法,实现对疾病的全面认知和精准诊断。其核心价值在于模拟多学科会诊模式,充分利用各类医疗数据的互补性。 -
概念重组:
多模态AI是把多种模态的医疗数据进行智能化分析,通过模态间的融合实现整体认知。 -
上下文关联:
文章通过介绍多模态AI的发展背景、技术架构、应用场景和挑战,系统性地阐述了这一技术在医疗领域的应用价值和发展前景。 -
规律分析:
主要矛盾:数据整合与临床应用之间的矛盾
次要矛盾:
- 数据标准化问题
- 隐私安全问题
- 模型解释性问题
- 临床验证问题
- 功能分析:
核心功能:辅助医生进行更全面、准确的临床决策
定量指标:
- 诊断准确率提升6.2个百分点
- 数据维度:平均2-3种模态
定性指标: - 诊断全面性提升
- 决策可解释性增强
- 来龙去脉梳理:
- 起因:医疗数据爆发式增长,单一模态AI无法满足临床需求
- 发展:多模态AI技术不断演进,从简单特征融合到深度学习方法
- 现状:已在多个医学领域取得应用,但仍面临多个技术和实践挑战
- 趋势:向更智能、可解释、易部署的方向发展
通过这样的分析,我们可以更全面地理解多模态AI在医疗领域的应用价值和发展方向。
1. 确认目标
如何利用多模态AI技术提升医疗诊断的准确性和可靠性?
2. 分析过程(目标-手段分析)
主问题:如何整合多源医疗数据以提供更全面的临床决策支持?
子问题拆解:
-
如何处理不同模态数据的特征提取?
- 使用专门的编码器:CNN用于图像、RNN用于序列数据
- 采用预训练模型:降低特征提取难度
- 自监督学习:处理未标注数据
-
如何实现不同模态数据的有效融合?
- 早期融合:数据层面直接合并
- 中期融合:特征层面整合
- 晚期融合:决策层面组合
-
如何处理模态缺失问题?
- 数据补全:使用插值或生成方法
- 灵活架构:设计可处理缺失模态的模型结构
- 迭代优化:通过重建损失等方式提高鲁棒性
3. 实现步骤
-
数据预处理
- 标准化处理
- 缺失值处理
- 数据对齐
-
模型设计
- 特征提取模块
- 模态融合模块
- 预测输出模块
-
训练与验证
- 多任务学习
- 交叉验证
- 外部验证
4. 效果展示
目标:提升医疗诊断准确性
过程:多模态数据整合与分析
问题:数据异质性、模态缺失
方法:深度学习特征提取与融合
结果:相比单模态提升6.2个百分点
数字:432篇相关研究分析
5. 领域金手指
- 公共数据集驱动
- TCGA:14%研究使用
- ADNI:8%研究使用
- MIMIC:5%研究使用
这些数据集成为推动领域发展的"金手指",因为:
- 提供标准化数据
- 支持跨机构研究
- 便于结果复现
- 促进方法比较
实际案例:
- 神经系统:阿尔茨海默病诊断
- 呼吸系统:肺癌预后预测
- 消化系统:结直肠癌分期
- 生殖系统:乳腺癌预后评估
这些案例都依赖公共数据集进行方法验证和性能评估,展示了"金手指"在推动领域发展中的关键作用。
上述分析揭示了多模态AI在医疗领域的系统性解决方案,从问题分解到实际落地都有清晰的思路和可行的方法。通过公共数据集这一"金手指",可以更好地推动相关研究和应用的发展。
结构分析
1. 层级结构分析
叠加形态(从基础到高级)
-
数据层
- 基础医疗数据(影像、病理、临床记录)
- 预处理数据(标准化、对齐)
- 特征数据(编码后的表示)
-
技术层
- 特征提取(CNN、ViT、RNN)
- 模态融合(早期、中期、晚期)
- 预测决策(诊断、预后、治疗)
-
应用层
- 辅助诊断
- 预后预测
- 治疗规划
构成形态(部分到整体)
└── 多模态AI系统
├── 数据处理模块
│ ├── 影像处理单元
│ ├── 文本处理单元
│ └── 组学数据处理单元
├── 模型架构模块
│ ├── 特征提取器
│ ├── 融合器
│ └── 决策器
└── 临床应用模块
├── 诊断支持
├── 风险评估
└── 治疗建议
分化形态(从一到多)
- 医疗数据来源分化
- 影像科:CT、MRI、超声
- 病理科:切片图像
- 临床科:症状记录、检验报告
2. 线性结构分析(发展趋势)
2018年 → 2024年的演进:
- 数据规模:小规模单中心 → 大规模多中心
- 模型复杂度:简单融合 → 深度学习架构
- 应用范围:单一任务 → 多任务协同
- 验证方式:内部验证 → 外部验证
- 整体发展:实验室研究 → 临床应用
3. 矩阵结构分析
纵轴:医学专科
横轴:技术特征
| 专科领域 | 数据类型 | 主要应用 | 性能提升 | 验证程度 |
|---|---|---|---|---|
| 神经系统 | MRI+临床 | 诊断预测 | +6.2% | 高 |
| 呼吸系统 | CT+文本 | 预后评估 | +5.8% | 中 |
| 消化系统 | 病理+组学 | 分期分类 | +4.9% | 中 |
| 生殖系统 | 影像+临床 | 风险预测 | +5.2% | 低 |
4. 系统动力学分析
核心要素及其关系:
-
推动力
- 数据增长
- 技术进步
- 临床需求
-
阻力
- 数据孤岛
- 隐私安全
- 验证难度
-
反馈环
正向:- 模型改进 → 性能提升 → 临床认可 → 数据积累
负向: - 复杂度增加 → 解释难度 → 临床质疑 → 应用受限
- 模型改进 → 性能提升 → 临床认可 → 数据积累
通过这四种结构分析方法的组合,我们可以:
- 理解系统的层次性(层级分析)
- 把握发展方向(线性分析)
- 定位具体应用(矩阵分析)
- 预测系统演化(系统动力学)
这种多维度的分析帮助我们更全面地理解多模态AI在医疗领域的应用现状和未来发展趋势。
观察和假设
1. 关键观察
不寻常的现象
-
论文数量变化:
- 2018年仅3篇
- 2024年激增至150篇
- 观察:增长速度异常快
-
数据模态组合:
- 影像+文本(206篇)远超其他组合
- 影像+病理(16篇)数量意外偏少
- 观察:模态组合分布极不均衡
-
性能提升:
- 多模态平均提升6.2%
- 部分研究提升显著(>10%)
- 部分几乎无提升(<1%)
- 观察:性能提升差异巨大
2. 变量分析
发生变化的因素
-
数据可用性:
- 公共数据集规模扩大
- 数据共享平台增多
- 数据标准化程度提高
-
技术演进:
- 预训练模型普及
- 融合策略多样化
- 计算资源提升
-
临床需求:
- 诊断复杂度增加
- 精准医疗要求提高
- 多学科协作加强
3. 假设提出
主要假设
-
数据驱动假设:
“公共数据集的可用性是决定研究方向的关键因素”- 证据:神经系统研究最多(122篇),恰好有ADNI等大型数据集
- 验证:其他领域研究数量与数据集可用性高度相关
-
技术瓶颈假设:
“影像+病理研究少是由于数据对齐难度大”- 证据:需要复杂的配准技术
- 验证:成功案例多采用特殊的对齐策略
-
性能差异假设:
“模态互补性决定了性能提升空间”- 证据:信息重叠度低的模态组合提升更显著
- 验证:通过信息熵分析验证互补程度
-
发展趋势假设:
“实际临床应用是制约发展的主要瓶颈”- 证据:FDA认证产品极少
- 验证:多数研究停留在实验阶段
4. 验证方向
-
针对数据驱动假设:
- 统计数据集可用性与研究数量的相关性
- 分析新数据集发布对研究方向的影响
-
针对技术瓶颈假设:
- 研究成功案例的技术路线
- 分析失败案例的具体障碍
-
针对性能差异假设:
- 计算不同模态间的信息冗余度
- 分析性能提升与模态特性的关系
-
针对发展趋势假设:
- 追踪临床试验进展
- 分析监管审批要求
通过这种观察-假设-验证的分析框架,我们可以更好地理解多模态AI医疗应用的发展规律和关键制约因素,从而为未来研究方向提供指导。
解法拆解
1. 逻辑拆解
技术:
- 多模态医疗AI = 特征提取层 + 模态融合层 + 决策输出层
问题:
- 单一模态数据无法满足复杂医疗决策需求
- 不同模态数据的异构性和缺失问题
主要区别:
- 单模态 vs 多模态
- 独立决策 vs 协同决策
- 局部信息 vs 全局视角
子解法拆解:
-
特征提取子解法(因为数据异构性)
- CNN处理影像(因为空间结构特征)
- RNN处理序列(因为时序关联特征)
- Transformer处理文本(因为语义依赖特征)
-
模态融合子解法(因为信息互补性)
- 早期融合(因为原始数据相关性)
- 中期融合(因为特征层级一致性)
- 晚期融合(因为决策层面独立性)
-
缺失处理子解法(因为数据不完整性)
- 数据补全(因为统计规律性)
- 灵活架构(因为模态可变性)
- 注意力机制(因为重要性差异)
例子:
肺癌诊断中结合CT影像(解析肿瘤形态)、病理切片(分析细胞特征)和临床指标(评估风险因素)
2. 逻辑链结构
多模态AI解决方案
├── 数据预处理
│ ├── 标准化
│ └── 对齐
├── 特征提取
│ ├── 影像特征
│ ├── 文本特征
│ └── 组学特征
├── 模态融合
│ ├── 早期融合
│ ├── 中期融合
│ └── 晚期融合
└── 决策输出
├── 诊断预测
└── 预后评估
3. 隐性方法分析
发现的隐性方法:
-
特征重要性自适应
- 关键步骤:动态调整不同模态权重
- 定义:基于数据质量和任务相关性的自适应权重分配机制
-
跨模态知识迁移
- 关键步骤:利用一个模态的知识指导另一个模态的学习
- 定义:模态间的知识蒸馏和迁移学习方法
4. 隐性特征分析
发现的隐性特征:
-
模态协同度
- 特征表现:不同模态信息的互补程度
- 影响:决定融合策略的选择
-
时空一致性
- 特征表现:数据采集的时间和空间对应关系
- 影响:影响数据对齐和融合效果
5. 潜在局限性
-
技术局限:
- 模态对齐难度大
- 计算复杂度高
- 解释性不足
-
数据局限:
- 高质量多模态数据稀缺
- 标注成本高
- 隐私安全风险
-
应用局限:
- 临床验证不足
- 部署成本高
- 可扩展性受限
这种多层次的分析不仅帮助我们理解多模态AI的技术本质,也揭示了其在实际应用中的挑战和机遇。
全流程
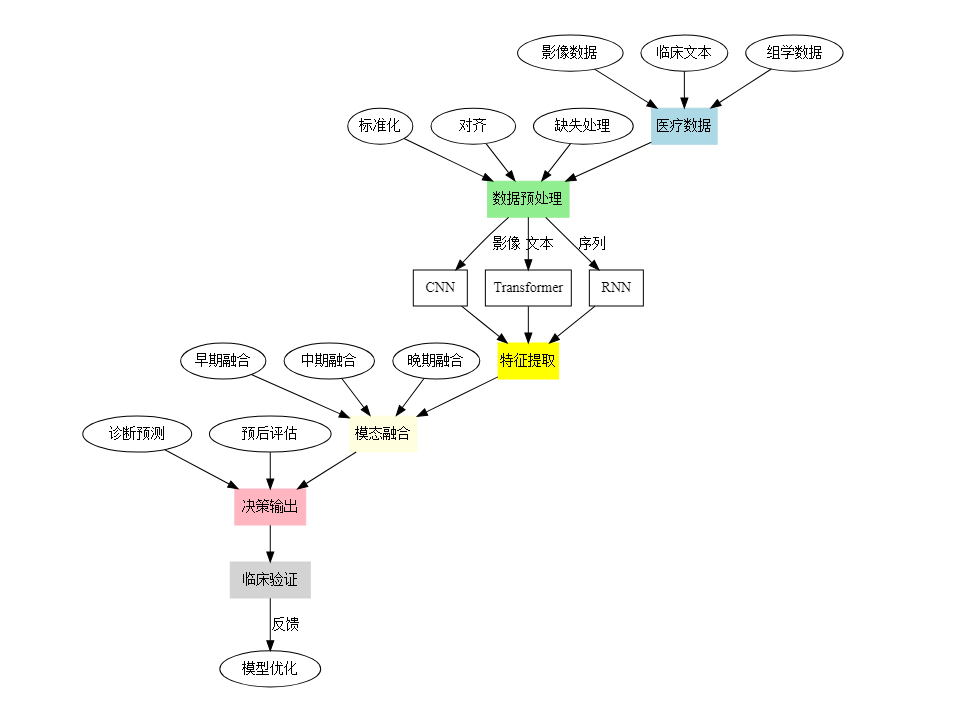
全流程优化分析
多题一解案例
-
共用特征:数据异构性
- 解法:模态特定编码器
- 适用场景:任何多模态数据融合任务
-
共用特征:数据缺失
- 解法:灵活架构设计
- 适用场景:不完整数据集分析
一题多解案例
以诊断任务为例:
-
早期融合解法
- 特征:原始数据相关性强
- 例:CT+核磁联合分析
-
晚期融合解法
- 特征:模态独立性强
- 例:影像+临床指标结合
优化方案
-
数据层优化:
- 原始:单一时间点数据
- 优化:纵向数据收集
- 效果:提升时序特征捕获
-
特征层优化:
- 原始:独立特征提取
- 优化:交互式特征学习
- 效果:增强模态间信息交流
-
融合层优化:
- 原始:固定融合策略
- 优化:自适应融合机制
- 效果:提高模型鲁棒性
输入输出示例
医疗场景:肺癌诊断
输入:
- CT影像序列
- 病理切片图像
- 临床检验报告
- 患者基本信息
处理流程:
-
数据预处理
- CT标准化
- 病理图像分割
- 文本向量化
-
特征提取
- CT:ResNet50提取特征
- 病理:Vision Transformer
- 文本:BERT编码
-
模态融合
- 特征级注意力机制
- 交叉模态自注意力
-
决策生成
- 多任务学习头
- 不确定性估计
输出:
-
主要输出
- 诊断结果(良恶性)
- 置信度分数
- 预后预测
-
辅助输出
- 关键区域热图
- 决策依据说明
- 建议后续检查